|
|
BMe Kutatói pályázat |
|
Oláh György Doktori Iskola
BME Vegyészmérnöki és Biomérnöki Kar, Szerves Kémia és Technológia Tanszék
Témavezető: Dr. Csontos István
Elektrosztatikus szálképzéssel előállított anyagok folyamatos feldolgozása
A kutatási téma néhány soros bemutatása
A hatásos gyógyszerjelöltek száma évről évre növekszik a korszerű molekulakeresési és tesztelési módszereknek köszönhetően. Az ígéretes hatóanyagok nagy része azonban rossz vízoldhatósággal jellemezhető, ezáltal a szervezetben való kioldódásuk és biológiai hasznosulásuk alacsony, ami gátolja az engedélyeztetésüket és forgalomba hozatalukat. A kioldódás javítására egy kiváló módszer az elektrosztatikus szálképzés, mely egy gyors, kíméletes, folyamatos technológia megfelelő hatóanyag-leadású nano- vagy mikrométeres átmérőjű szálak előállítására. Az előnyös tulajdonságok ellenére a módszert a gyógyszeriparban még csak kutatási területeken alkalmazzák. Ennek fő oka, hogy a szálas anyagok hatékony és biztonságos méretnövelt gyártása, feldolgozása és a végső gyógyszerforma kialakítása még nem teljesen megoldott. Kutatómunkám céljául ezért azt tűztem ki, hogy folyamatos úton, több technológiai lépést összekapcsolva állítsak elő szálakat tartalmazó tablettákat. Továbbá célom volt, hogy roncsolásmentes analitikai módszerekkel folyamatosan nyomon kövessem a gyártást, biztosítva ezzel az állandó termékminőséget.
A kutatóhely rövid bemutatása
A BME Vegyész és Biomérnöki Kar Szerves Kémia és Technológia Tanszékén működő FirePharma kutatócsoport a gyógyszeripar területén innovatív, nemzetközi érdeklődést kiváltó témákkal foglalkozik, melyekből számos publikáció került közlésre rangos folyóiratokban. Csoportunk kapcsolatban áll és közös projektekben vesz részt hazai és külföldi gyógyszercégekkel, illetve akadémiai kutatócsoportokkal.
A kutatás történetének, tágabb kontextusának bemutatása
Napjainkban a potenciális gyógyszerjelöltek jelentős hányada jellemezhető rossz vízoldhatósággal, így a szervezetben nem oldódnak ki megfelelően és ez sok esetben alacsony biológiai hasznosuláshoz vezet. Az oldhatósági problémák kezelésére ezért számos megoldást dolgoztak ki az évek során, melyek közül kiemelhető az amorf szilárd diszperziók előállítása és alkalmazása [1]. Az amorf forma kialakításával a hatóanyag kémiai szerkezetének megváltoztatása nélkül növelhető a látszólagos oldhatóság, aminek köszönhetően a gyógyszerjelölt biológiai hasznosulása úgy javulhat, hogy az eredeti hatása is megmarad. Az amorf szilárd diszperziók alkalmazásának sikerét jelzi, hogy 2017-ig 24 ilyen típusú gyógyszert fogadott el az amerikai gyógyszerhatóság [2].
Az amorf szilárd diszperziók előállítására számos technológiai megoldást fejlesztettek ki az évek során, melyek közül egy nagyon hatékony módszer az oldószeres elektrosztatikus szálképzés. A technológia gyógyszeripari alkalmazásához azonban elengedhetetlen a méretnövelés és a nano-, illetve mikrométeres átmérővel jellemezhető szálas termékek feldolgozása és a leggyakoribb gyógyszerforma, a tabletta kialakítása [3,4]. Továbbá előnyös lenne, ha az elektrosztatikus szálképzéssel előállított amorf szilárd diszperziókból folyamatos technológiai lépéseken keresztül alakítanák ki a végső gyógyszerformát, ezzel csökkentve a gyártási időket, a költségeket és a gyártósor helyigényét. A folyamatos technológiákat és az azokhoz kapcsolható gyors, roncsolásmentes analitikai módszereket egyre jobban támogatják a gyógyszerügyi hatóságok is. Különböző irányelvekkel ösztönzik a gyógyszercégeket ezek alkalmazására, hiszen így a gyártások sokkal szabályozottabbá, biztonságosabbá és hatékonyabbá tehetők [5].
Az amorf szilárd diszperziók és a folyamatos technológiák együttes alkalmazásával elérhető a rossz vízoldhatóságú hatóanyagokat tartalmazó, állandó minőségű tabletták hatékony, környezetbarát és biztonságos előállítása. Ennek eredményeként a betegek számára sokkal több hatásos gyógyszerkészítmény vállhat elérhetővé, miközben az előállításuk korszerű módszerekkel valósul meg.
A kutatás célja, a megválaszolandó kérdések
Bár az elektrosztatikus szálképzés gyógyszeripari alkalmazási lehetőségeit sokan kutatják, kevés példa található a szakirodalomban szálakat tartalmazó tabletták előállítására, folyamatos feldolgozásuk pedig még egyáltalán nem valósult meg. A kutatás során a célom éppen ezért az volt, hogy két rossz vízoldhatóságú hatóanyag, a spironolakton és az itrakonazol kioldódását javítsam elektrosztatikus szálképzés alkalmazásával, majd a szálakból folyamatos feldolgozási lépések útján tablettákat állítsak elő. Továbbá célom volt, hogy a kristályos nyomok és a hatóanyag-tartalom mérésére roncsolásmentes, a folyamatok mellé illeszthető analitikai módszereket fejlesszek, amelyekkel a szálas anyagot tartalmazó tabletták folyamatos előállítása során állandó termékminőség biztosítható.
Módszerek
Elektrosztatikus szálképzés
A szálak előállításához a tanszékünkön fejlesztett nagysebességű elektrosztatikus szálképző berendezéseket alkalmaztam. A spironolaktontartalmú minták esetén egy horizontális elrendezésű készüléket használtam, melynek kulcseleme egy rozsdamentes acél korong alakú szórófej volt. A szórófejen egyenlő távolságban elhelyezkedő furatokon keresztül áramlott ki az oldat, miközben a fej forgó mozgást végzett. A szórófejre nagyfeszültség volt kapcsolva, míg azzal szemben egy földelt gyűjtőlemez helyezkedett el. Az így keletkező potenciálkülönbség és a szórófej forgó mozgása miatt fellépő centrifugális erők hatására a fejből kilépő folyadéksugár megnyúlt, elvékonyodott, az oldószer pillanatszerűen elpárolgott, és a földelt gyűjtőn nano- és mikrométeres átmérőjű szálak keletkeztek. Az itrakonazoltartalmú szálak esetén egy vertikális elrendezésű nagysebességű elektrosztatikus szálképzőt használtam, mely közvetlenül kapcsolódott egy szálak gyűjtésére alkalmas ciklonhoz (1. ábra). Ez a berendezés megfelelő környezetbe telepítve kielégítheti a GMP (Good Manufacturing Practice: Jó Gyártási Gyakorlat) követelményeket, mely a gyógyszeriparban kulcsfontosságú szempont. Az oldatok adagolását mindkét esetben perisztaltikus pumpával végeztem.
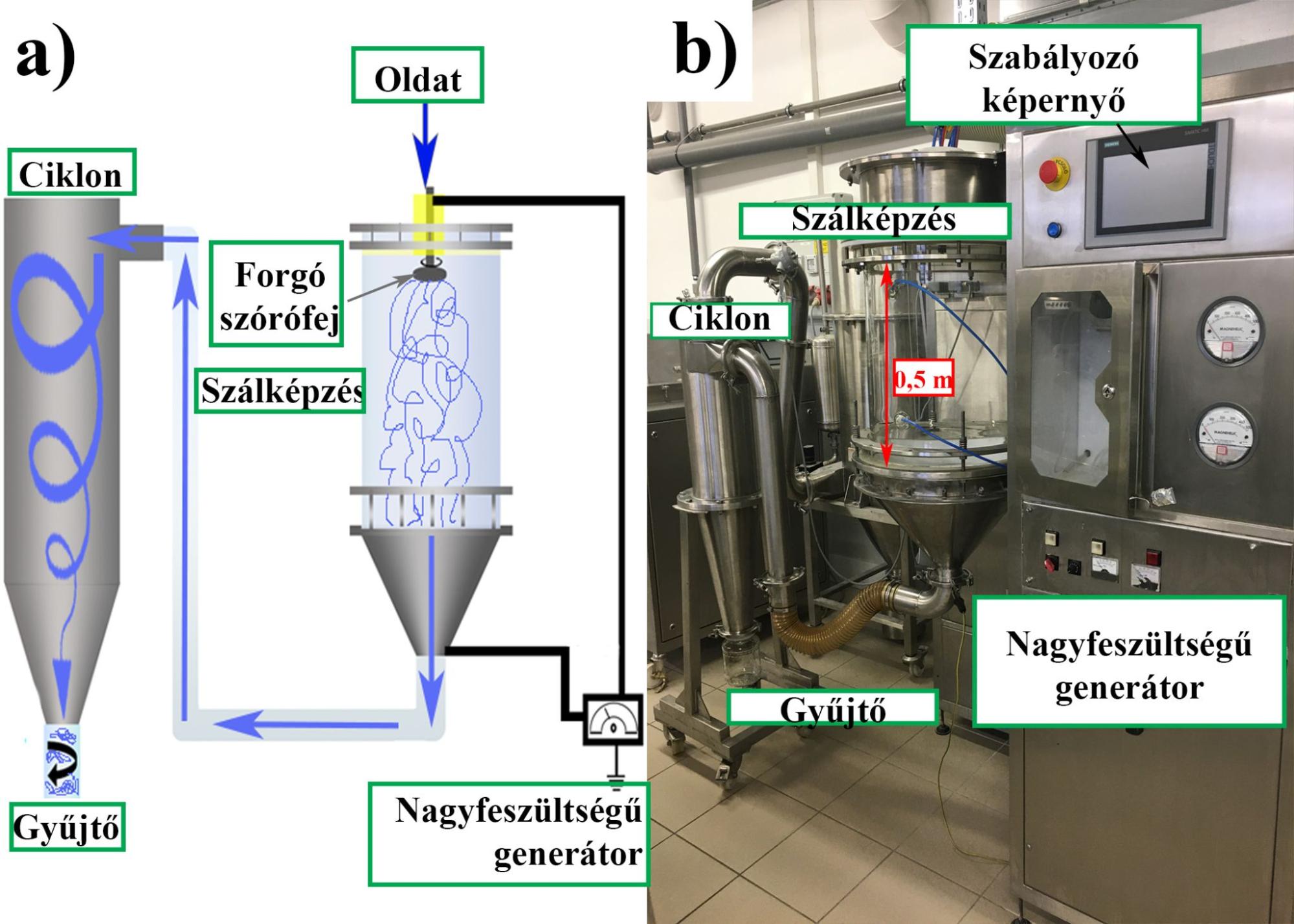
1. ábra: Nagysebességű elektrosztatikus szálképző ciklonnal összekapcsolva (sematikus ábra (a) és fénykép (b))
Szálak feldolgozása
A szálas termékek gyűjtésére a spironolaktontartalmú minták esetén egy tanszékünkön fejlesztett berendezést használtam, melyen három forgó henger segítette a gyűjtőanyag folyamatos mozgatását, míg a készülék alján egy orvosi penge végezte a szálak folyamatos eltávolítását. Az itrakonazoltartalmú szálak folyamatos gyűjtésére az 1. ábrán látható ciklont használtam. A szálak őrlését a spironolaktontartalmú minták esetén egy 0,8 mm átmérőjű szitával végeztem, míg az itrakonazoltartalmú termékek esetén egy 2 mm-es szita átmérőjű oszcillációs őrlőt használtam. Az adagolási kísérletekhez egy gravimetrikus módban üzemeltethető ikercsigás adagolót, illetve egy vibrációs adagolót használtam. A folyamatos homogenizálást egy ikercsigás extruder segítségével hajtottam végre, melytől egy futószalag szállította el a porkeveréket a tablettázó felé. Mindkét esetben egy excenteres tablettázó gépet használtam a szálas anyagot tartalmazó tabletták előállításához.
Analitikai módszerek
A szálakat vizsgáltam pásztázó elektronmikroszkópiával, differenciális pásztázó kalorimetriával, por-röntgendiffrakcióval, termogravimetriával és egy UV–Vis (ultraibolya látható) spektrofotométerrel összekapcsolt kioldó készülékkel. A részecskeméret-eloszlás meghatározásához lézerdiffrakciós módszert alkalmaztam. Vizsgáltam továbbá a porkeverékek tömörített és tömörítetlen halmazsűrűségét, valamint a tabletták törési szilárdságát, kopását, vastagságát és nedvességtartalmát.
Ezeken kívül folyamatos rendszerek mellé illeszthető, in-line alkalmazható, roncsolásmentes analitikai módszereket is használtam, melyek a közeli infravörös (near infrared: NIR-) és a Raman-spektroszkópia voltak. A kristályos nyomok és a hatóanyag-tartalom méréséhez kalibrációs modelleket fejlesztettem MATLAB szoftver segítségével.
Eddigi eredmények
Nagysebességű elektrosztatikus szálképzés alkalmazásával több mint harmincszoros termelékenység növekedés volt elérhető a spironolaktontartalmú szálak előállítása esetén. A szálak folyamatos gyűjtésére alkalmasnak bizonyult a tanszékünkön fejlesztett készülék, a termékek jól őrölhetők voltak. Nagy szemcseméretű mikrokristályos cellulózzal homogenizálva a szálas terméket 385 g/óra adagolási sebességgel lehetett adagolni a porkeveréket egy ikercsigás gravimetrikus adagolóval. További segédanyagokkal homogenizálva a porkeveréket sikeresen állítottam elő tablettákat, melyeknél a kioldódás mértéke hasonlított a tiszta szálas termékek eredményeihez. Megállapítottam, hogy a kristályos hatóanyag-tartalom a kioldódás csökkenését eredményezi, ezért a kristályos nyomok vizsgálatára NIR- és Raman-spektroszkópiás módszereket fejlesztettem. A legjobb kalibrációs eredményeket a porkeverékek Raman-spektroszkópiás vizsgálatából kaptam, ami igazolta, hogy ez a módszer jól alkalmazható lehet egy folyamatos gyártás során a termék minőségének folyamatos vizsgálatához. Az elvégzett kísérletek és eredményeik rávilágítottak arra, hogy az elektrosztatikus szálképzéssel előállított hatóanyag-tartalmú termékek folyamatos feldolgozása lehetséges, azonban a megfelelő minőség biztosításához elengedhetetlen a folyamatok mellé illeszthető, gyors analitikai módszerek fejlesztése (2. ábra).
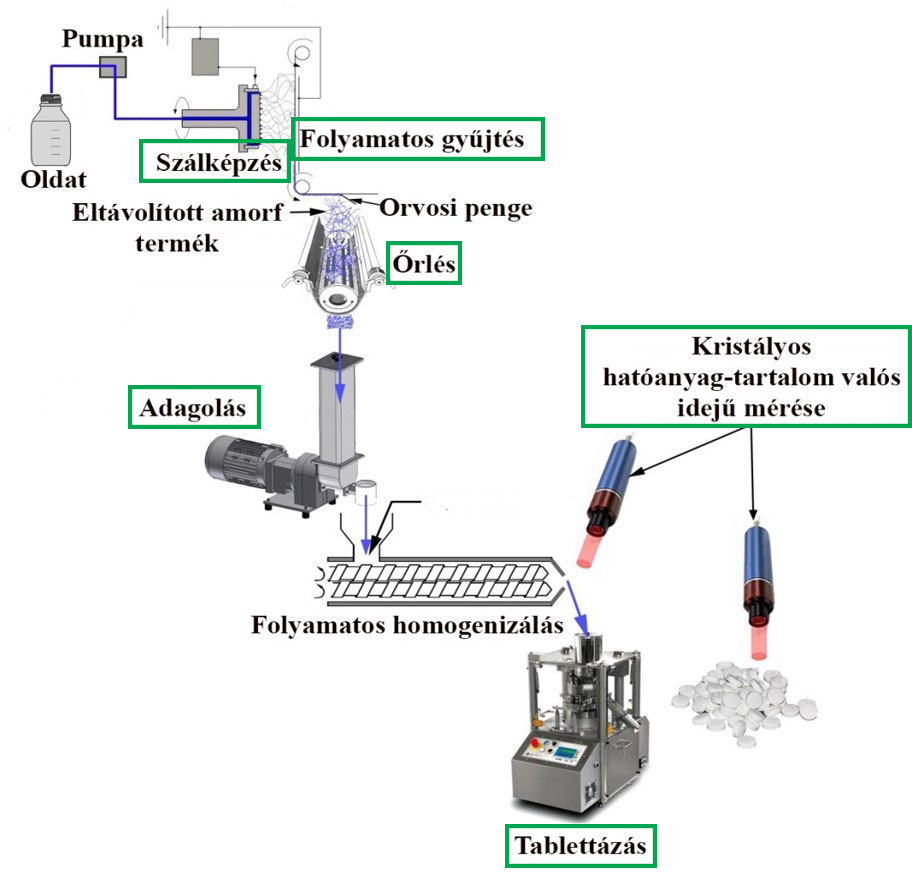
2. ábra: Az elektrosztatikus szálképzésen alapuló folyamatos feldolgozási rendszer lehetséges lépései. (A zölddel kiemelt lépések voltak részletesen vizsgálva a kísérletek során.)
A kutatómunka következő lépésében a folyamatos homogenizálás és tablettázás megvalósítása volt a cél, amelyhez itrakonazolt tartalmazó szálakat állítottam elő (3. ábra).

3. ábra: Az itrakonazoltartalmú szálakat tartalmazó tabletták folyamatos előállítására kidolgozott integrált rendszer sematikus rajza.
A szálak folyamatos gyűjtését egy ciklon alkalmazásával valósítottam meg, melynek alján elhelyezett gyűjtőben a szálak folyamatos forgó mozgást végeztek (4. ábra).

4. ábra: A ciklon alján elhelyezett gyűjtőben a szálak folyamatos forgó mozgást végeztek.
Bár a gyűjtőedényben a forgó mozgás hatására a szálak folyamatosan őrlődtek, a jobb gördülékenység és kezelhetőség eléréséhez további őrlési lépés alkalmazására volt szükség, melyre alkalmasnak bizonyult a folyamatos gyártásba is beilleszthető oszcillációs őrlés. A következő lépésnél a szálakat sikerült segédanyagok nélkül egy vibrációs adagoló használatával egy folyamatos homogenizálásra alkalmas ikercsigás extruderbe adagolni, míg egy ikercsigás gravimetrikus adagolóval a segédanyagok keverékét juttattam a rendszerbe (5. ábra).

5. ábra: A folyamatos homogenizáláshoz összeállított rendszer.
A homogenizálásból érkező porkeverék szálas anyag tartalmát NIR- és Raman-spektroszkópiával sikerült folyamatosan mérni (6. ábra), melyből a hatóanyag-tartalom is könnyen meghatározható volt. Végül a porkeveréket egy futószalag a tablettázó készülékbe szállította. A folyamat végén az elkészített tabletták hatóanyag-tartalmát szintén sikeresen meg tudtam határozni NIR- és Raman-spektroszkópia alkalmazásával. A referencia módszerként alkalmazott UV–Vis-spektrofotometriás mérés pedig alátámasztotta a két roncsolásmentes analitikai módszer eredményeit.
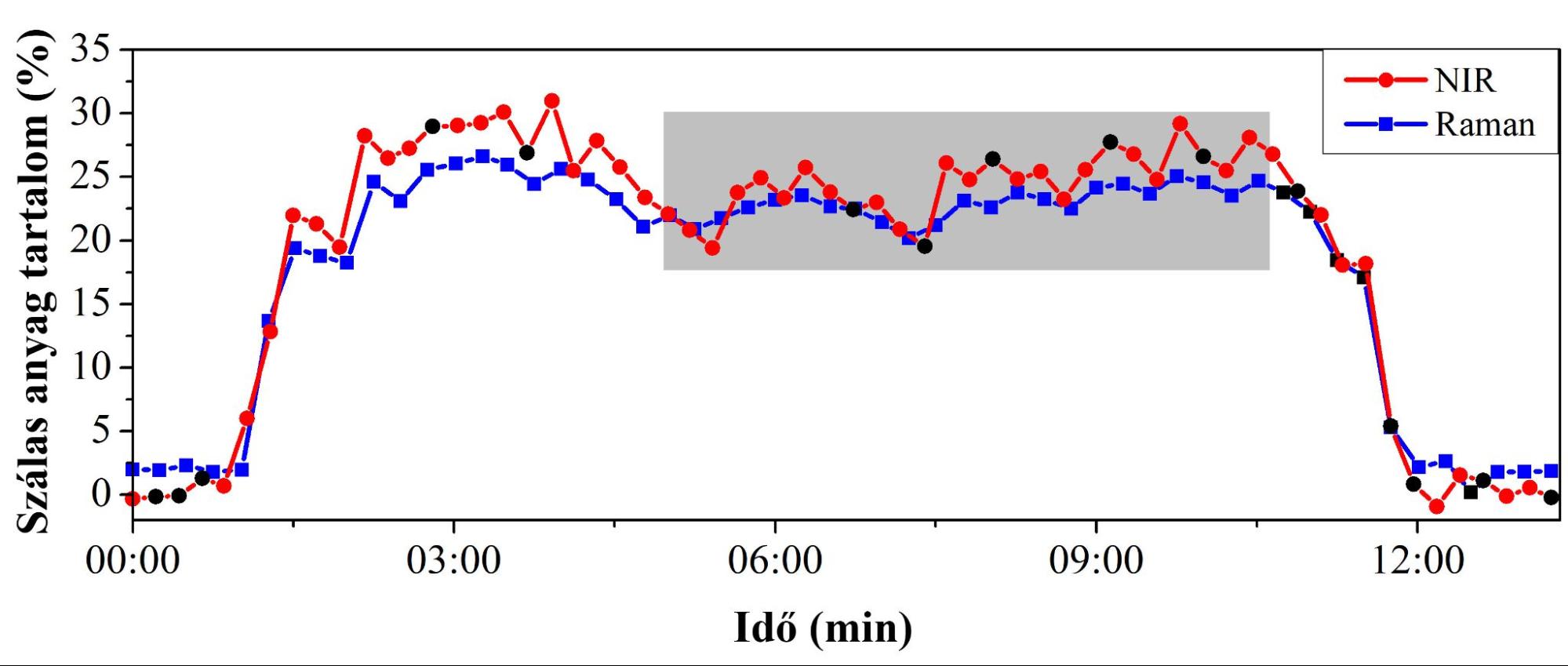
6. ábra: A folyamatos homogenizálás nyomon követése NIR- és Raman-spektroszkópiával. (A szürkével kiemelt rész jelzi az állandósult állapot elérését.)
Várható impakt, további kutatás
Kutatómunkám eredményei rávilágítottak arra, hogy az elektrosztatikus szálképzéssel előállított termékek folyamatos feldolgozása lehetséges, aminek köszönhetően lehetővé válik a rossz vízoldhatóságú gyógyszerjelöltek kioldódásának javítása és a tabletta forma kialakítása hatékony, gyors és biztonságos úton. A munka jelentős része a Felsőoktatási és Ipari Együttműködési Központ (FIEK) projekt keretein valósult meg, melynek során a Richter Gedeon Nyrt. munkatársaival dolgoztunk együtt. Továbbá a munka egyes részei a Janssen (Johnson & Johnson gyógyszeripari vállalata) kutatóival együttműködésben valósultak meg. Ezek az együttműködések mind arra utalnak, hogy a tématerület iránt jelentős az ipari érdeklődés, és az eredmények hasznosítása a közeljövőben megvalósulhat.
A kutatás folytatásában vizsgálom a szálas termékek folyamatos granulálásának lehetőségeit, illetve az amorf szilárd diszperziók stabilitását befolyásoló tényezőket, hogy a tabletta- vagy a kapszulaforma kialakítása még hatékonyabb és könnyebb legyen.
Saját publikációk, hivatkozások, linkgyűjtemény
Kapcsolódó saját publikációk listája (IF: impakt faktor, C: hivatkozások)
[I] E. Szabó, B. Démuth, B. Nagy, K. Molnár, A. Farkas, B. Szabó, A. Balogh, E. Hirsch, G. Marosi, Z.K. Nagy, Scaled-up preparation of drug-loaded electrospun polymer fibres and investigation of their continuous processing to tablet form, Express Polymer Letters, 12(5) (2018), 436-451
IF: 2,875 C: 27
[II] E. Szabó, B. Démuth, D.L. Galata, P. Vass, E. Hirsch, I. Csontos, G. Marosi, Z.K. Nagy, Continuous formulation approaches of amorphous solid dispersions: Significance of powder flow properties and feeding performance, Pharmaceutics, 11(12) (2019), 654
IF: 4,421 C: 10
[III] E. Szabó, P. Záhonyi, D. Brecska, D.L. Galata, L.A. Mészáros, L. Madarász, K. Csorba, P. Vass, E. Hirsch, J. Szafraniec-Szczęsny, I. Csontos, A. Farkas, G. Van den Mooter, Z.K. Nagy, G. Marosi, Comparison of amorphous solid dispersions of spironolactone prepared by spray drying and electrospinning: The influence of the preparation method on the dissolution properties, Molecular Pharmaceutics, 18(1) (2021), 317–327
IF: 4,939 C: 0
[IV] E. Szabó, P. Záhonyi, M. Gyürkés, B. Nagy, D.L. Galata, L. Madarász, E. Hirsch, A. Farkas, S.K. Andersen, T. Vígh, G. Verreck, I. Csontos, G. Marosi, Z.K. Nagy, Continuous downstream processing of milled electrospun fibers to tablets monitored by near-infrared and Raman spectroscopy, European Journal of Pharmaceutical Sciences, 164 (2021), 105907
IF: 4,384 C: 0
[V] P. Vass, E. Szabó, A. Domokos, E. Hirsch, D. Galata, B. Farkas, B. Démuth, S.K. Andersen, T. Vigh, G. Verreck, G. Marosi, Z.K. Nagy, Scale‐up of electrospinning technology: Applications in the pharmaceutical industry, Wiley Interdisciplinary Reviews: Nanomedicine and Nanobiotechnology, 12(4) (2020), e1611
IF: 9,182, C: 53
[VI] B. Démuth, D.L. Galata, E. Szabó, B. Nagy, A. Farkas, A. Balogh, E. Hirsch, H. Pataki, Z. Rapi, L. Bezúr, T. Vigh, G. Verreck, Z. Szalay, Á. Demeter, G. Marosi, Z.K. Nagy, Investigation of deteriorated dissolution of amorphous itraconazole: Description of incompatibility with magnesium stearate and possible solutions, Molecular Pharmaceutics, 498 (2017), 234–244
IF: 4,556 C: 14
[VII] B. Démuth, D.L. Galata, A. Balogh, E. Szabó, B. Nagy, A. Farkas, E. Hirsch, H. Pataki, T. Vígh, J. Mensch, G. Verreck, Z.K. Nagy, G. Marosi, Application of hydroxypropyl methylcellulose as a protective agent against magnesium stearate induced crystallization of amorphous itraconazole, European Journal of Pharmaceutical Sciences, 121 (2018), 301–308
IF: 3,532 C: 8
[VIII] P. Vass, E. Hirsch, R. Kóczián, B. Démuth, A. Farkas, C. Fehér, E. Szabó, Á. Németh, S.K. Andersen, T. Vígh, G. Verreck, I. Csontos, G. Marosi, Z.K. Nagy, Scaled-up production and tableting of grindable electrospun fibers containing a protein-type drug, Pharmaceutics, 11(7) (2019), 329
IF: 4,421 C: 13
[IX] P. Vass, Z.K. Nagy, R. Kóczián, C. Fehér, B. Démuth, E. Szabó, S.K. Andersen, T. Vígh, G. Verreck, I. Csontos, G. Marosi, E. Hirsch, Continuous drying of a protein-type drug using scaled-up fiber formation with HP-β-CD matrix resulting in a directly compressible powder for tableting, European Journal of Pharmaceutical Sciences, 141 (2020), 105089
IF: 4,384 C: 12
[X] G. Fülöp, A. Domokos, D.L. Galata, E. Szabó, M. Gyürkés, B. Szabó, A. Farkas, L. Madarász, B. Démuth, T. Lendér, T. Nagy, D. Kovács-Kiss, F. Van der Gucht, G. Marosi, Z.K. Nagy, Integrated twin-screw wet granulation, continuous vibrational fluid drying and milling: A fully continuous powder to granule line, International Journal of Pharmaceutics, 594 (2021), 120126
IF: 5,875 C: 3
Linkgyűjtemény
Szerves Kémia és Technológia Tanszék
Hivatkozások listája
[1] G. Van den Mooter, The use of amorphous solid dispersions: A formulation strategy to overcome poor solubility and dissolution rate, Drug Discov. Today, 9(2) (2012), e79-e85
[2] S.V.Jermain, C. Brough, R.O. Williams III, Amorphous solid dispersions and nanocrystal technologies for poorly water-soluble drug delivery – An update, Int. J. Pharm., 535(1–2) (2018), 379–392
[3] Z.K. Nagy, A. Balogh, B. Démuth, H. Pataki, T. Vígh, B. Szabó, K. Molnár, B.T. Schmidt, P. Horák, G. Marosi, G. Verreck, I. Van Assche, M.E. Brewster, High speed electrospinning for scaled-up production of amorphous solid dispersion of itraconazole, Int. J. Pharm., 480(1–2) (2015), 137–142
[4] B. Démuth, Z.K. Nagy, A.Balogh, T.Vígh, G.Marosi, G.Verreck, I.Van Assche, M.E. Brewster, Downstream processing of polymer-based amorphous solid dispersions to generate tablet formulations, Int. J. Pharm., 486(1–2) (2015), 268–286
[5] S.L. Lee, T.F. O’Connor, X. Yang, C.N. Cruz, S. Chatterjee, R.D. Madurawe, C.M. V Moore, L.X. Yu, J. Woodcock, Modernizing pharmaceutical manufacturing: from batch to continuous production, J. Pharm. Innov. 10 (2015) 191–199.
